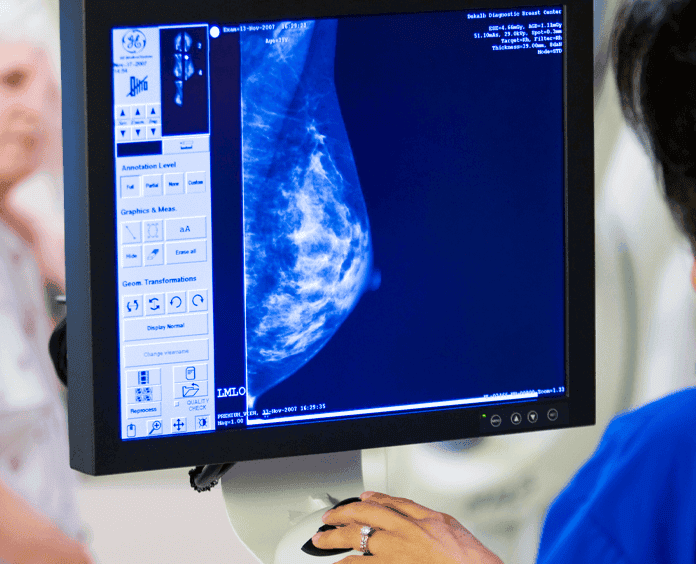
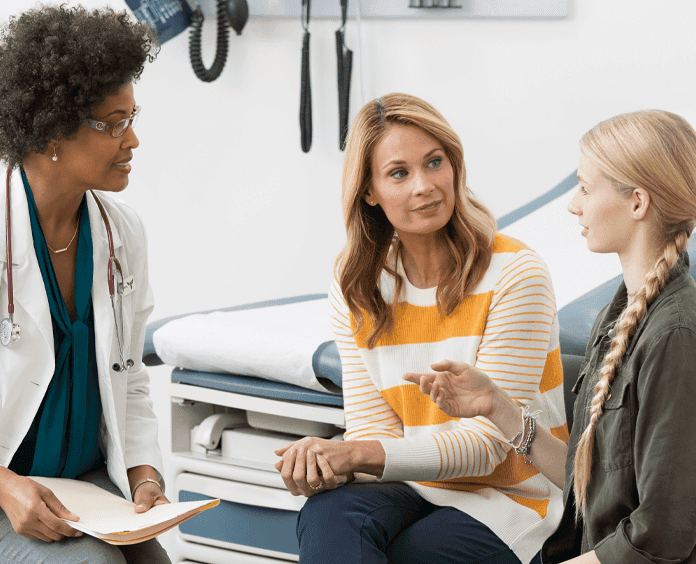Cada cáncer. Cada vida.
La American Cancer Society es la organización líder en la lucha contra el cáncer con la visión de acabar con el cáncer tal como lo conocemos, por el bien de todos. Somos la única organización que mejora las vidas de las personas con cáncer y de sus familias combatiendo el cáncer por medio de la defensa, investigación y apoyo al paciente, para asegurar que todas las personas tengan la oportunidad de prevenir el cáncer, de combatirlo con tratamiento y de sobrevivir a él.
Temas destacados
Entender el tipo de pólipos puede prevenir el cáncer de colon.
Examine su piel periódicamente, y sabrá lo que es normal en su caso.
Descarga ACS CARES™ para obtener recursos.
Honre la memoria de su ser querido por un mundo sin cáncer.
Información y recursos sobre el cáncer
A 1 de cada 3 hombres y mujeres se les diagnosticará cáncer en el transcurso de su vida. Si le han diagnosticado cáncer hace poco, o conoce a alguien que tiene cáncer, contamos con respuestas, orientación y apoyo.
Servicios a su disposición
En la American Cancer Society ofrecemos todo tipo de apoyo para los pacientes, las familias y los cuidadores.
Impacto general de la American Cancer Society
Ayúdenos a continuar nuestra tarea ⏵
Riesgo, prevención y pruebas de detección
Usted puede ayudar a reducir el riesgo que corre de tener cáncer mediante decisiones saludables, tales como tomar una alimentación adecuada, mantenerse en activo y no fumar. También es importante seguir las recomendaciones para las pruebas de detección, con las que se pueden detectar ciertos tipos de cáncer en una etapa temprana.
Voluntariado y recaudación de fondos
Lo que hacemos no sería posible sin el apoyo de nuestros voluntarios, recaudadores de fondos y donadores. Juntos, marcamos la diferencia, y usted también puede hacerlo. Colabore en servicios de voluntariado, realice un donativo deducible de impuestos o participe en un evento de recaudación de fondos para ayudarnos a salvar vidas.
Impacto del voluntariado y la recaudación
Participe en actividades de voluntariado o de recaudación de fondos
Investigación que salva vidas
¿Qué se requiere para vencer al cáncer? Investigación. Desde 1946, hemos invertido más de USD $5 mil millones en investigación del cáncer, todo para encontrar y mejorar tratamientos, descubrir factores que pueden causar cáncer y mejorar la calidad de vida de las personas con cáncer.