Cada cáncer. Cada vida.
La American Cancer Society es la organización líder en la lucha contra el cáncer con la visión de acabar con el cáncer tal como lo conocemos, por el bien de todos. Somos la única organización que mejora las vidas de las personas con cáncer y de sus familias combatiendo el cáncer por medio de la defensa, investigación y apoyo al paciente, para asegurar que todas las personas tengan la oportunidad de prevenir, combatir con tratamiento y sobrevivir el cáncer.
Temas destacados
¿Se puede heredar el cáncer?
Descubra lo que se sabe sobre la genética y el riesgo de cáncer.
Para quienes cuidad de alguien con cáncer
Un diagnóstico de cáncer impacta no solo al paciente sino a familiares y amigos
Pon en marcha tus ganas de hacer el bien
Participa como voluntario para conducir a personas al lugar de tratamiento del cáncer.
Su donativo para conmemorar
Honre la memoria de su ser querido para un mundo libre de cáncer.
Directo a información del cáncer
Cáncer y recursos informativos
Uno de cada dos hombres y una de cada tres mujeres, será diagnosticado(a) con cáncer en el transcurso de su vida. Si recientemente usted o alguien a quien conoce ha recibido un diagnóstico con esta enfermedad, contamos con respuestas a sus preguntas, al igual que orientación y apoyo.
Servicios a su disposición
Impacto en términos generales
Apreciamos todo el apoyo que recibimos ⏵
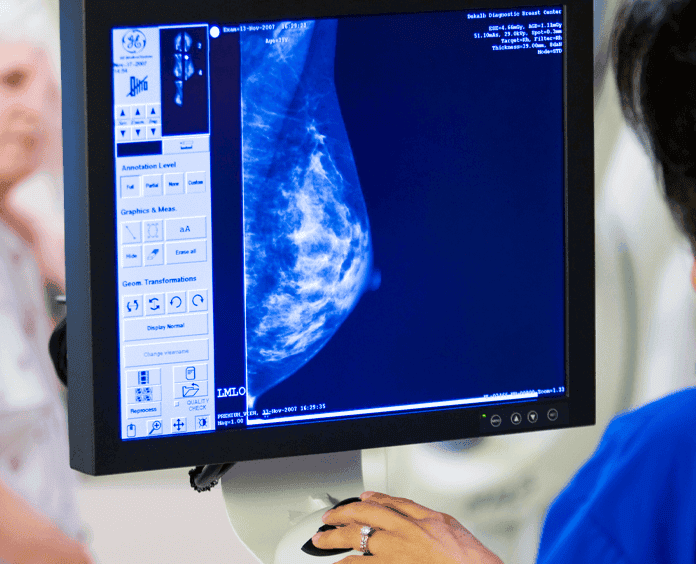
Riesgo, prevención y pruebas de detección
Usted puede ayudarse a reducir su propio riesgo al tomando decisiones que fomentne un estilo de vida saludable, como lo es una alimentacipon sana, mantenerse fisicamente activo(a) y no fumar. También es importante seguir las recomendaciones para hacer las pruebas de detección del cáncer que le correspondan, lo cual ayuda a detectar el cáncer en sus etapas inciales.
Voluntariado y recaudación de fondos
Lo que logramos hacer no sería posible sin el apoyo de nuestros voluntarios, recaudadores y donadores. Juntos, estamos haciendo la diferencia, ¡y usted podría apoyarnos también! Únase como voluntario(a), contribuya con su donativo deducible de impuestos o participe en uno de nuestros eventos para la recaudación de fondos, con lo cual nos ayudaría a salvar vidas.
Impacto del voluntariado y la recaudación
Participe como voluntario y/o apoyándonos en eventos para la recaudación de fondos
Investigación que salva vidas
¿Qué se requiere para vencer al cáncer? Investigación. Desde 1946, hemos invertido más de USD $4.9 mil millones en nuestra búsqueda de nuevos y mejores tratamientos, descubrir factores que pueden ser causantes de cáncer y mejorar la calidad de vida de las personas que afrontan esta enfermedad.